九强生物2021年年度董事会经营评述
2022-04-26 19:43:53 来源: 同花顺金融研究中心
九强生物(300406)2021年年度董事会经营评述内容如下:
一、报告期内公司所处行业情况
根据中国证监会《上市公司行业分类指引》的规定,公司所处行业属于制造业(C)中的医药制造业(分类代码:C27),根据行业细分,公司属于医药制造业中的“体外诊断行业”。(一)行业概况体外诊断是指在人体之外,通过对人体样本(各种体液、细胞、组织样本等)进行检测而获取临床诊断信息,进而判断疾病或机体功能的产品和服务。体外诊断在疾病治疗过程中,对提高病因诊断准确性、合理选择治疗方案、合理评价疗效等方面,都发挥着越来越重要的作用。根据中国生物技术发展中心发布的《我国体外诊断产业现状及发展建议》显示,临床诊断信息80%以上来自于体外诊断。20世纪80年代以来,随着科学技术的快速发展,随着现代生物技术、单克隆抗体技术、微电子处理器、光化学等方面的重要突破,目前全球已形成了一个保持3%-6%的年增长率的持续发展的产业。根据Grand View Research的统计,2019年全球体外诊断市场规模约为725亿美元,2020年由于受到新冠肺炎疫情的影响,约为834亿美元,同比扩大15.03%。我国体外诊断行业起步于20世纪80年代,行业增长速度居世界前列。经过三十几年的发展,我国体外诊断行业现已具备一定的市场规模和基础,目前仍处于快速成长期。根据医疗器械研究院发布的《中国医疗器械蓝皮书(2021)》数据显示,2020年,中国体外诊断市场规模达890亿元,同比增长24.3%。一方面,相对于发达国家,我国体外诊断产业起步相对较晚,虽然经过最近几年的快速发展,我国体外诊断市场规模有所提升,但与欧美成熟市场相比,市场规模差距依然很大,增长潜力巨大。另一方面,随着我国政府对医药卫生事业的重视、医药卫生支出增加、三胎全面开放和人口结构老龄化加速所带来的医疗保健高消费人数增加以及分级诊疗制度建设的推进,基层医疗机构对IVD产品和服务的需求不断增加。根据Frost &Sullivan研究预测,2019-2024年,中国体外诊断行业市场规模将保持超越医药行业平均的增速,以18.8%的复合增长率快速增长。我国体外诊断市场整体的快速发展,也为国内体外诊断企业特别是已经具有一定规模和竞争优势的企业提供了广阔发展空间。生化诊断是IVD领域发展最早、最成熟的细分行业。生化诊断是临床检测最常用的技术手段之一,一般以生化试剂配合开放式的分析仪器,通过测定特定的生化物质,如蛋白质/酶类、代谢底物类、糖类、脂类、无机离子类的含量反映肝功能、肾功能、心功能、胰腺功能、体液免疫系统的健康状况。生化诊断由于具有检验成本低、操作简便、检测速度快、精密度高、重复性好、检测结果不受操作影响的优势以及较为成熟的市场运作模式,相关产品除了在欧美日等发达国家具有扎实的消费基础外,在包括中国在内的印度、巴西、南非等新兴国家市场中也得到了快速推广。根据美国IQVIA(前IMS,Health &Quintiles)披露的数据,2019年生化诊断市场在全球IVD市场中占比约为15%,位列第三位。(二)市场格局体外诊断行业已成为在全球范围内拥有数百亿美元庞大市场容量的成熟行业,市场集中度较高。目前行业内企业主要分布在北美、欧洲等体外诊断市场发展较早、容量较大的经济发达国家和地区,据IVD Technology统计,美国、西欧和日本为全球前三大体外诊断市场,市场份额分别为41%、25%、9%,发达国家市场相对成熟,发展较为平稳。以Roche(罗氏)、Abbott(雅培)、Beckman Coulter(贝克曼-库尔特;Danaher(丹纳赫)旗下公司)、Siemens(西门子)为主的“4+X”形成了较为稳定的市场格局;行业前十的公司销售收入均在10亿美元以上,其产品线十分丰富,不仅包括各类体外诊断试剂,还包括各类诊断仪器以及与之相关的医疗技术服务,且在各自细分领域都极具竞争力,占据全球八成的市场份额。从全球范围来看,IVD市场集中度较高,而与此同时,国内市场的集中度偏低。据前瞻产业研究院研究显示,就国内体外诊断市场的竞争格局来看,2017年占据市场超过5%份额的5家海外巨头组成了体外诊断行业的第一梯队,共占据国内市场36.8%的市场份额,其产品性能好、检测精密度高,主要占据国内三级医院等高端市场;其次,国内优质的体外诊断公司组成了第二梯队,虽然在经营规模和产品种类方面稍逊于海外巨头,但随着我国体外诊断行业的快速增长,国内体外诊断龙头也在飞速成长当中;最后,国内一大批中小型企业组成了第三梯队,600家企业共占据约40%的市场,市场占有率较低,规模效益不明显。由于我国体外诊断产业发展起步较晚,部分体外诊断企业存在资金实力不强、技术研发投入不足、综合竞争实力较弱等情况。目前我国IVD行业的生产企业约有300-400家,行业集中度低。近几年来,随着我国体外诊断市场需求快速增长,国内规模较大的企业抓住机遇,凭借产品性价比高和更为贴近本土市场的优势,不断抢占份额,致使原以进口产品为主导的市场格局被逐渐打破,一批优秀企业也通过加大研发投入、加强国际合作、借助上市再融资等方式,不断做大做强,提升自身综合竞争力及其产品的国际市场影响力和知名度,积极参与国际市场竞争,并在某些产品领域逐渐具备与国际巨头竞争的实力。目前国内各领域领先企业正积极进行多元化发展,主要有以下五个发展特点:一是细分领域排名靠前的企业依托已形成的竞争优势向体外诊断的其他细分领域渗透,以丰富产品种类;二是试剂厂商增加仪器生产和仪器配套能力,仪器厂商增加试剂生产能力,以增强市场竞争实力;三是开始积极开拓海外市场;四是一些以提供第三方检验实验室的企业出现在行业中;五是一些非IVD生产型的商业企业,通过委托医院耗材采购及整合销售渠道,快速抢占市场份额。随着国内领先企业技术研发实力的提升和经营规模的壮大,可以预期行业市场集中度将进一步提高,同时国内领先企业与国外企业在高端市场的竞争能力也将快速提升。(三)行业壁垒技术壁垒:体外诊断产业是典型的高技术密集型产业,其产品技术横跨微电子、机械设计与制造、计算机技术、临床医学、生物医学工程、医学检验、材料学、有机化学等众多学科,产品技术含量高、研发资金投入大、开发周期长,生产工艺流程复杂、质量控制要求高,提高了进入本行业的技术壁垒。人才壁垒:高技术密集型产业的特点要求企业拥有更多的跨领域交叉学科复合型技术人才。由于国内体外诊断行业起步较晚,复合型人才相对缺乏,只能通过企业自身多年的培养与积累。新进入的企业很难在短时间内培养及招聘具有核心技术的复合型科研人才,形成新进入者的人才壁垒。资金壁垒:资金需求主要体现在三个方面,对研发生产条件与设备的要求较高,投入较大;产品技术升级换代较快,持续研发投入资金巨大;建设专业的、覆盖面广的营销网络与售后服务体系需要大量资金投入。上述三点形成对新进入者较大的资金壁垒。营销渠道壁垒:体外诊断产品专业性强,需要企业培养专业的营销人才队伍和专业的售后服务人才队伍;营销网络和技术服务网络建设周期长、资金投入大;国际知名诊断企业已经在国内形成多年的市场垄断,增加了国内企业产品进入市场的难度,形成了对新进入者的营销渠道壁垒。质量与品牌壁垒:体外诊断产品的检测结果直接为临床医生对疾病的诊断及疗效评价提供准确依据,产品质量是临床检验机构选择产品首要考虑的因素;国际知名诊断企业十多年的市场营销推广确立了进口诊断产品在国内临床检验机构的品牌优势、诊断标准,形成了对新进入者较高的质量与品牌壁垒。市场准入壁垒:国内体外诊断企业实行生产和经营许可证管理制度,国家监管部门对生产和经营企业的生产设备、场地、从业人员资质等方面有较高要求;国家监管部门对体外诊断产品实行产品注册证许可制度,企业从产品研发、临床试验、研发现场考核和质量管理体系现场审核,直至许可上市需要较长的时间,形成对新进入企业的市场准入壁垒。二、报告期内公司从事的主要业务公司需遵守《深圳证券交易所上市公司自律监管指引第4号——创业板行业信息披露》中的“医疗器械业务”的披露要求(一)主营业务简介北京九强生物技术股份有限公司是一家以生化诊断试剂(“金斯尔”品牌试剂)和肿瘤病理检测试剂的研发、生产和销售为主营业务的高成长型企业,目前拥有生化检测系统、血凝检测系统、血型检测系统和免疫病理染色系统。生化领域,公司现已建立起化学法、酶法(含循环酶法)、普通免疫比浊法、胶乳增强免疫比浊法、克隆酶供体酶免疫测定技术(CEDIA)、酶增强免疫测定技术(EMIT)等生化研发平台;基于底物显色法、比浊法、凝固法的血凝检测试剂研发平台和其配套的仪器研发/生产平台和基于微柱凝胶法的血型试剂及配套仪器研发平台。在肿瘤病理领域,公司产品基本覆盖医院病理科日常肿瘤病理诊断和鉴别诊断所需试剂和免疫组化全自动化病理染色系统,并已建立起单克隆抗体制备技术、全自动化病理检测系统和荧光原位杂交等分子病理检测试剂/仪器研究平台,积极向分子病理诊断领域拓展并探索多元化服务和技术路线。(二)公司医疗器械证书情况及其用途公司自成立以来一直致力于体外诊断试剂的研发、生产和销售,是我国体外诊断行业的领先企业,也是我国生化诊断试剂品种最齐全的生产厂商之一。尤其是在高端诊断试剂(如胱抑素C、同型半胱氨酸、小而密低密度脂蛋白胆固醇)领域,公司在国内处于领先水平。公司目前的主要诊断试剂种类有肝功类、肾功类、血脂类、心肌损伤、特种蛋白和糖代谢类生化指标,以及血栓与止血监测和血型监测指标等。公司自有品牌“金斯尔”是行业内知名品牌,产品覆盖体外生化诊断试剂的大多数项目,主要产品包括胱抑素C、同型半胱氨酸、胆汁酸(TBA)、载脂蛋白A1、载脂蛋白B、小而密低密度脂蛋白胆固醇、肌酸激酶同工酶(mass法)等生化诊断试剂;以及D-Dimer, FDP, AT-III 为代表的出凝血检测诊断试剂及其配套MDC3500全自动血凝仪组成的封闭检测系统;以ABO正反定型卡,抗筛卡为代表的血型检测诊断试剂;和一抗、二抗等免疫组化试剂产品等。公司体外诊断试剂按照功能不同可以分为以下11大类:2021年1-12月,公司共获得167项产品注册证变更批件,完成49项产品延续。取得28项新产品注册证,取得12项新产品备案凭证,有77项新产品在注册过程中,有5项产品在变更注册过程中。其中九强生物共获得110项产品注册证变更批件,完成49项产品延续。取得28项新产品注册证,并有77项新产品在注册过程中;子公司迈新生物共获得49项产品备案变更批件。取得12项新产品备案凭证,并有5项产品在变更注册过程中;子公司美创新跃共获得8项产品注册证变更批件。具体情况如下:(1)九强生物1.处于注册申请中的医疗器械2.获得注册证的医疗器械3.报告期末医疗器械注册证数量224个,去年同期197个。(2)迈新生物1.处于变更注册申请中的医疗器械2.获得注册证/备案凭证的医疗器械3.报告期末迈新生物医疗器械注册证数量5个,去年同期5个;医疗器械备案凭证证数量317个,去年同期305个。(3)美创新跃1.获得注册证的医疗器械2.报告期末美创新跃医疗器械注册证数量8个,去年同期8个。(三)公司的主要经营模式为适应公司快速发展的需要,公司建立了国际一流的产品生产环境及生产管理流程,秉承“质量第一”的准则,向市场提供涵盖临床生化及血液领域的高品质临床检测项目,能针对不同目标客户提供多元化的临床诊断解决方案。同时,公司更加重视终端的用户体验,遍及全国的技术服务团队,保证在第一时间为用户解决疑难,提供完备的技术服务支持。“与巨人同行”。自2013年起,九强生物与雅培、罗氏、日立、迈瑞、威高等国内外知名企业陆续建立起生化战略合作关系,与雅培签署的《技术许可和转让合作协议》更是开创了中国IVD企业技术输出的先河。通过十多年的长足发展,九强生物已经成长为中国领先的体外诊断产品生产厂商,并逐步在国际IVD市场上占有一席之地。(四)公司的参考测量平台公司于2008年开始建立参考体系运行部门,负责参考测量方法的建立及运行、公司常规测量系统的溯源和定值工作。参考系统部建立了紫外可见分光光度计和液相色谱串联质谱(LC-MS)两大参考测量平台,将近20项参考测量程序,每年参加国际临床化学协会(IFCC)主办,德国临床化学和实验室协会(DGKL)承办的国际参考实验室能力比对(RELA)和国家卫健委组织的医学参考实验室质量评价活动(EQARL),取得了优异成绩,同时,2016年公司开展了国家认证委员会(CNAS)医学参考实验室认可工作,截止目前共有12个项目通过了CNAS(ISO17025和ISO15195)医学参考实验室认可。经过多年运行验证,技术成熟,方法稳定,结果可靠。利用参考系统部的技术和方法,参考系统部完成了将近150项产品量值溯源,为公司产品测量结果的准确可靠提供了更有力的保障。(五)公司的质量管理体系运行情况公司依据质量管理体系标准ISO13485和国家医疗器械相关法规要求建立了质量管理体系,每年进行内审和管理评审,不断持续改进,保证产品质量。2021年共接收外部审核11次,各级药监机构及第三方审核机构审核共8次,第二方供应商审核3次,审核结果均合格。(六)报告期内主要的业绩驱动因素(1)公司通过公开摘牌取得迈新生物30%股权,迈新生物已办理完成了股权收购的相关工商变更登记手续。本次收购完成后,公司持有迈新生物 95.55%股权。目前,本公司在迈新生物原有业务良好发展的基础上,对其市场、渠道、研发及管理等方面进行资源优化配置,实现互利共赢协同发展。(2)公司投资北京中科纳泰科技有限公司,持股5.1387%,并签署了《独家经销框架协议》。中科纳泰主营业务为循环肿瘤细胞体外诊断技术的研发及相关产品的生产和销售,提供肿瘤早筛早诊、动态监控、用药指导等个体化精准服务。关键技术即中科纳泰自主研发的“肿瘤捕手”高灵敏度多肽纳米磁珠捕获外周血循环肿瘤细胞技术,该技术创新地利用微纳米开发了高通量微流控多肽合成技术,基于微流控技术的高亲和力和高特异性靶向多肽筛选,实现了CTC的高效富集检测。中科纳泰拥有该核心技术的专利权,该技术对于实现我国肿瘤液体活检的医学诊断、精准治疗和生命科学研究完全自主知识产权,具有重要的临床应用价值和市场竞争意义。本次合作关系的建立,使公司进入了新的业务领域,拓宽了公司销售的产品线,对公司的业务布局将起到积极作用。(3)2021年,公司及控股子公司迈新生物入选了国家工业和信息化部第三批专精特新“小巨人”企业名单。(4)公司取得医用版的抗原卡取得了CE认证,新型冠状病毒抗体检测试剂盒(胶乳免疫比浊法)在意大利等国已有销售,积极拓展海外新冠业务,全力支持全球新冠防控。三、核心竞争力分析2021年提升公司竞争力方面的主要工作一、研发能力持续提升,主要表现在以下3个方面:(1)研发投入持续增加。研发的持续投入,是研发工作取得进展的基础条件。2021年公司的研发投入127,008,278.01元,较2020年增加了60.66%。研发团队稳定。公司研发团队日趋成熟,核心研发人员稳定、未发生变化,为未来持续研发成果的出现奠定基础(2)2021年公司取得了丰硕的研发成果,共获得及申请了64项专利;1.九强生物获得的专利2.迈新生物获得的专利二、加强品牌建设,向产品国际化迈进。(1)加强品牌建设1.公司非常重视品牌建设,视质量为品牌的基础。在研发体制中,推行“质量始于研发”的理念,并将客户、供应商(特别是原料供应商)、公司技术支持体系、质量控制体系与研发体系组合成一个有机整体,从而提高产品与服务质量,为品牌建设打下牢固基础;2.根据“品牌首先应在内部人员心目中竖立”的理念,公司强化了与品牌相关的培训活动,特别是新产品重点内容的培训并通过考核体系将培训内容落实到实处;3.强化对客户的服务,公司除了不断扩大试剂应用的技术服务队伍之外,为了配合自有生化系统的而销售,扩大了仪器工程部的人员规模,为客户提供全方位的软硬件服务,受到客户一致好评。(2)与巨人合作提升竞争力为实现公司与巨人共行----与行业内领先企业紧密合作的发展战略。2021年度与雅培(中国)的合作进展良好,雅培(中国)继续向九强生物采购生化产品。2017年签署的补充协议里新增十多个项目,第一批目前已经完成上市,最后3个项目预计将在2022年4月份完成上市;在2021新增雅培Alinity c平台的合作项目32个,将分三批完成上市,预计32个项目中的第一批产品将于2022年6月上市。与雅培国际的合作正在按计划进行,进展顺利。公司与法国ELITechGROUP公司(以下简称“ELITech”)在签署的《战略合作意向书》基础上,双方正在评价公司的一些生化产品,由于疫情原因,原计划的商务洽谈和公司参观现在待定,但目前和Elitech公司高层保持良好的沟通,等疫情结束,商务可以正常外来,马上启动参观和实质合作。公司利用ELITech既有的销售渠道及新开拓的客户渠道对公司生化诊断产品加速引入全球市场具有重要意义。三、加强营销网络建设,销售持续增长。(1)2021年公司实现营业收入1,599,384,352.43元,比上年度增长88.58%(2)为落实公司“精耕细作”的销售战略,管理层2021年重点开展了以下几个方面的工作:强化计划与考核管理、强化新产品培训、强化管理层对基层营销网络的巡视指导活动、优化经销商网络布局,提高区域经销商销售效率。四、推出九强生物自有品牌的生化分析系统及凝血分析系统,完善战略领域产品线布局目前,公司在全面的生化检测菜单基础上不断推陈出新,完善的分析测量程序将优势产品与主流生化仪器品牌紧密连接,同时不断提升自有的G92000和G9800两款生化分析封闭系统的市场占有率。同期,公司推出了MDC7500和MDC3500两款全自动凝血分析仪,并积极推进流水线及配套试剂项目研发,分别满足高中低端客户的需求。2021年公司加大了自有生化及凝血分析系统的销售力度,进一步挖掘扩大生化诊断市场潜力、布局抢占凝血诊断市场,为未来市场份额的维护和增长奠定基础。五、公司积极布局生化诊断以外的细分检验领域1.公司投资高端血凝分析系统研发及产业化项目,包括前期厂房建设资金,项目总投资20929万元,资金均公司自有资金。项目主要研究内容是立足于核心技术平台,通过对凝固法、免疫法、发色底物法等关键技术的突破,在血凝分析检测领域开展创新能力建设,领先国际水平,实现国产凝血诊断试剂及凝血高端分析仪器的研发及产业化。加快中国制造替代进口产品的步伐,为国内医疗机构降低检测成本,填补国内空白,提高国产血凝产品在高端市场上的占有率及国际市场的竞争力,为国家血栓与止血性疾病诊断提供高性价比的优质产品和服务。该项目的实施能提升公司血凝仪器产品线的研发能力,同时扩大公司血凝仪器的生产规模,增强公司盈利能力和抗风险能力,提升公司综合竞争力。2.布局基层医疗市场,POCT(即时检验)产品,其操作简单,检测周期短,能对患者实施连续监测、诊断、管理和筛查,外来应用、发展空间广泛。公司于2021年成立POCT研发组,搭建POCT研发、规模化生产平台,依托募投项目研发中心及参考实验室的建设加大产品研发的投入力度、加快产品注册的时间进度,该平台的建立填补了九强生物快速检测试剂的空白,本公司正全力以赴、争分夺秒以丰富的有竞争力的POCT产品支持国内外销售业绩快速增长。六、公司积极进行外延式并购,矢志成为体外诊断全产品线供应商公司通过公开摘牌取得迈新生物30%股权,迈新生物已办理完成了股权收购的相关工商变更登记手续。本次收购完成后,公司持有迈新生物95.55%股权。目前,本公司在迈新生物原有业务良好发展的基础上,对其市场、渠道、研发及管理等方面进行资源优化配置,实现互利共赢协同发展。七、公司财务指标公司的盈利指标四、主营业务分析1、概述报告期内,全国疫情整体可控,医疗机构正常运行,公司业务恢复至正常水平,销售收入和利润增长。与此同时公司不断加大市场开拓力度,拓展销售渠道,寻求新的经济增长点。同时,以市场为导向,进一步加大研发投入,不断创新产品,丰富产品结构。1、本报告期,主营业务收入159,838.53万元,比上年同期84,724.00万元增长88.66%,从产品构成来看, 诊断试剂业务仍是主营业务收入主要来源,试剂收入占主营业务收入的92.64%。本报告期,经销模式收入占主营收入的60.88%,销售额较上年同期增长49.08%。直销收入占主营业务收入的39.12%,销售额比上年同期增长221.26%,主要原因是收购迈新生物导致,迈新生物以直销为主,经销为辅。2、公司实行以销定产的生产模式,以市场需求为导向,根据订货合同和以往的销售数据,结合库存情况,编制不同层次的生产计划。3、公司采购主要包括采购计划的制定、供应商的选择、采购价格的确定、质量控制四个环节,主要采购原材料、代理试剂及仪器。五、公司未来发展的展望2022年主要战略举措:1、企业与品牌管理。企业内部继续完善企业的管理体系和企业文化建设工作,从而提高企业的管理水平和效率;品牌方面,利用行业、学术会议和论坛,加强与宣传媒体的合作,进一步提升公司品牌形象,为销售、合作的拓展奠定良好的基础。2、资本运作。抓住行业整合的机遇,利用上市公司的优势并结合国药集团打造IVD工业平台的战略机遇,积极开展新产品线,尤其是分子病理、伴随诊断等方面的收购与投资。3、产品研发和产品注册。依托募投项目研发中心及参考实验室项目的建设加大产品研发的投入力度、加快产品注册的时间进度,全力以赴、争分夺秒以丰富的有竞争力的产品支持销售业绩快速增长,尤其加快血型卡、血凝产品线、肿标产品、POCT产品的注册进度。4、病理产品线战略。巩固已有的产品优势,品牌优势,加强仪器带动抗体销售策略,不断加强新产品的研发,同时加快分子产品线的并购布局和国际市场的开拓。5、质量控制体系。不断总结与国际大公司合作的经验,建立一流的质量控制体系标准。6、企业合作。国内合作:利用国内商业渠道的整合和商业模式发生的变化,积极开展与国药集团各省级公司以及国内强势经销商、打包托管商的紧密合作,从而快速拓宽销售渠道。国际合作:继续多方拓展销售渠道,贯彻“与巨人同行”战略,实现销售的有效增长。7、战略合作。利用好战略投资者国药投资带来的协同效应,加大与国药子公司的销售合作力度,推进公司业绩增长。8、新产品销售。2022年要加大宣传推广力度,同时争取更多省份取得收费,更重要的是在已经取得收费的地区努力实现销售,已经实现销售的地区要积极拓展销售范围,实现销售额的迅速增长。重点是继续推广小而密低密度脂蛋白、CK-MBmass和fPSA等产品。9、国际销售方面。加快高端团队建设,积极多方式开拓国际销售,包括品牌产品的销售、OEM产品的销售。10、公司自有生化系统的销售。公司已完成“仪器+试剂”的封闭生化系统的建设,为未来的发展奠定了坚实基础。2022年公司要加大推广、招商、促销力度,在选择重点省份推行九强自有生化分析系统的代理商体系,实现自有生化系统销售的突破。为公司持久发展打好基础。同时积极尝试以仪器合作为基础的医院检验科整体合作业务,提升销售增量。11、政府项目。利用“中关村国家自主创新示范区项目”等项目的契机,加强产品的研发、生产和销售。继续申报“国家企业技术中心”。12、招聘培训和营销管理。继续贯彻“精耕细作”的战略,优化销售区域管理,优化代理商管理,进一步细分销售区域和代理商管理。加大销售人员的招聘以及加强大区经理和业务人员的素质培训,严格日常管理,提升团队的执行力。热门资讯
-
九强生物2021年年度董事会经营评述
-
天津普林2021年年度董事会经营评述
-
泰恩康2021年年度董事会经营评述
-
华侨城A2022年一季度董事会经营评述
-
有方科技:预计2021年全年亏损1296.4万
-
科伦药业:预计半年度净利润同比增长35%至55%
-
复星医药2022年第一季度营收同比增长28.87%
-
惠理集团(00806)3月30日耗资约68.49万港元回购20万股
-
贵州三力(603439.SH)发布一季度业绩,净利润2373万元,同比增长1.23%
-
望变电气(603191.SH)将于4月28日在上交所上市
-
深交所向久量股份(300808.SZ)发出年报问询函 要求说明近两年营业收入、净利润持续下滑的具体原因
-
青海春天再亏损2.49亿,听花酒能让业绩“回甘”吗?|和讯曝财报
-
中核钛白(002145.SZ)2021年度净利润升156.03%至12.17亿元 拟10转4.5派0.8元
-
豫能控股(001896.SZ)拟投资建设河南鲁山抽水蓄能电站项目
-
中国神华(01088.HK):部分煤矿核增生产能力
-
百事(PEP.US)因涨价提高收入预期至8%
-
多国现不明原因肝炎,多家药企董秘回复肝炎治疗相关产品
-
华友钴业(603799.SH)拟推2022年员工持股计划 预计股份数量不超642.59万股
-
海容冷链(603187.SH)发布2021年业绩,净利润2.25亿元,同比减少16.02%,每10股派3元
-
深交所向立方数科(300344.SZ)发出年报问询函 要求说明收入确认和扣除是否合理合规
-
中恒集团(600252.SH)发布2021年业绩 净利润3.07亿元 同比降45.47% 每10股派0.27元
-
ISP GLOBAL(08487)发盈警,预期前三季度股东应占净亏损约150万新加坡元至190万新加坡元
-
歌尔股份(002241.SZ)发预盈,预计半年度净利润20.77亿元-24.23亿元,同比增长20%-40%
-
东杰智能:股东拟增持不低于35.00万股
-
业绩快报:洛阳钼业一季度净利17.92亿 同比增长77.88%
-
*ST昌鱼:预计2021年全年亏损2850.0万
-
亚邦股份2021年年度董事会经营评述
-
金钼股份2021年年度董事会经营评述
-
方大股份2021年年度董事会经营评述
-
春兰股份2021年年度董事会经营评述
-
上海电影2022年一季度董事会经营评述
-
开山股份2021年年度董事会经营评述
-
千禾味业2021年年度董事会经营评述
-
受益分布式光伏需求提升 锦浪科技2021年净利增长48.96%
-

圣迪乐成为中国航天事业合作伙伴
-
奥园美谷最新公告:下修2021年度业绩预告 预计亏损2.5亿元-3亿元
-
招商南油最新公告:拟以5000万元-1亿元回购股份
-
水发燃气2021年净利4121.78万同比增长72.3%董事长尚智勇薪酬66万
-
亚振家居2021年亏损6683.49万同比由盈转亏董事长高伟薪酬70.16万
-
鼎信通讯2021年净利1.57亿同比下滑13.49%董事长王建华薪酬366.34万
-
立霸股份2021年净利1.1亿同比增长14.85%董事长蒋达伟薪酬77.37万
-
健盛集团2021年净利1.67亿同比扭亏为盈董事长张茂义薪酬90万
-
海利尔2021年净利4.5亿同比增长10.59%董事长葛尧伦薪酬150.25万
-
乾照光电(300102.SZ)2020年净亏损2.47亿元 同比收窄11.81%
-
海峡环保2021年净利1.46亿同比增长12.62%总裁卓贤文薪酬58.57万
-
拓尔思(300229.SZ)与知识产权出版社签订战略合作协议
-
鼎龙股份(300054.SZ):4月26日首次回购320.94万股
-
联邦制药(03933.HK):注射用比阿培南通过仿制药质量和疗效一致性评价
-
华旺科技2021年年度董事会经营评述
-
拾比佰2021年年度董事会经营评述
-
中寰股份2021年年度董事会经营评述
-
大东南2021年年度董事会经营评述
-
奥园美谷:预计2021年全年亏损2.5亿至3.0亿
-
*ST索菱2021年年度董事会经营评述
-
江苏雷利2021年年度董事会经营评述
-
德林海2021年年度董事会经营评述
-
“转板第一股”观典防务在北交所终止上市 超1.7万户股东将变身科创板投资者
-

倍至斩获“德国iF设计大奖”!用专业呵护国人口腔健康
-
4月26日招商轮船跌5.35%,华泰柏瑞富利混合A基金重仓该股
-
4月26日新集能源跌9.98%,招商中证煤炭等权指数(LOF)A基金重仓该股
-
4月26日凤凰传媒跌5.40%,景顺长城沪港深精选股票基金重仓该股
-
4月26日中国核电跌5.07%,兴全趋势投资混合(LOF)基金重仓该股
-
4月26日晶方科技跌5.26%,大成积极成长混合基金重仓该股
-
4月26日中科曙光跌10.00%,天弘中证计算机ETF基金重仓该股
-
4月26日常熟汽饰跌9.98%,金鹰持久增利债券(LOF)C基金重仓该股
-
4月26日禾望电气跌5.44%,朱雀恒心一年持有混合基金重仓该股
-
4月26日万控智造跌9.99%,中银中证100ETF基金重仓该股
-
4月26日乐惠国际跌9.95%,中海消费混合基金重仓该股
-
4月26日新经典跌8.07%,嘉实新消费股票基金重仓该股
-
4月26日芯能科技跌5.98%,银河银泰混合基金重仓该股
-
4月26日金能科技跌6.28%,鹏华尊惠定期开放混合A基金重仓该股
-
4月26日海星股份跌8.12%,招商量化精选股票A基金重仓该股
-
4月26日保隆科技跌7.60%,光大优势配置混合基金重仓该股
-
4月26日江山欧派跌5.59%,长城久富混合(LOF)A基金重仓该股
-
4月26日兴通股份跌10.01%,国寿安保核心产业混合基金重仓该股
-
中石化油服(01033.HK):一季度净利下降58.8%至6829万元
-
思维列控(603508.SH):2021年净利扭亏为盈至3.85亿元 拟10转4派8.4834元
-
林海股份(600099.SH)2021年度净利润951.4万元 同比增长23.19%
-
日辰股份2021年年度董事会经营评述
-
华茂股份2021年年度董事会经营评述
-
天喻信息:预计2021年全年亏损1.35亿至1.55亿
-
中矿资源2022年一季度董事会经营评述
-
惠而浦称国美电器货款严重逾期终止合作 国美电器:随时可对账结算
-
“胶原+”战略有效推进 东宝生物2021年净利润同比增长97.74%
-
专访祥源新材总裁魏琼:新型发泡材料填补国内空白 切入新能源电池材料领域
-
元琛科技徐辉:围绕产业链做好环保文章
-
湖南一季度农业开局良好 早稻生猪成为农业亮点
-
博深股份2021年营收净利双增长 并购标的连续两年未完成业绩承诺
-

龙星化工拟非公开发行股票募资16.04亿元 用于产业项目建设
-

北流市新农人电商培训班开班 2021年网销超15亿元
-

广西兴业县开展“兴星之火”志愿服务活动 助力撂荒地复耕复种
-
雅戈尔25亿元增资夸父科技 加速推进“建时尚集团”战略愿景
-
通威股份累计建成18万吨高纯晶硅产能 达成阶段性产能目标
-
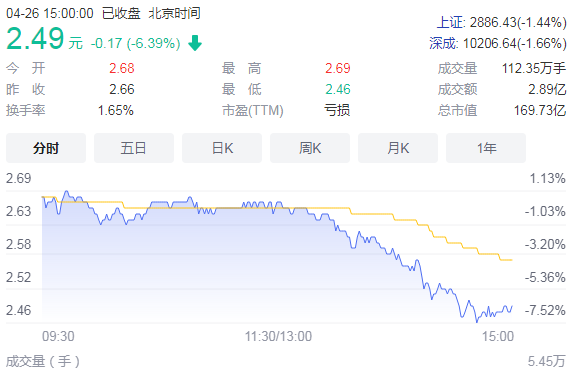
起拍价172.61亿元!太平洋第一大股东所持股份将被司法拍卖
-

灿瑞科技科创板IPO通过审核 关联交易和毛利率等被关注
-
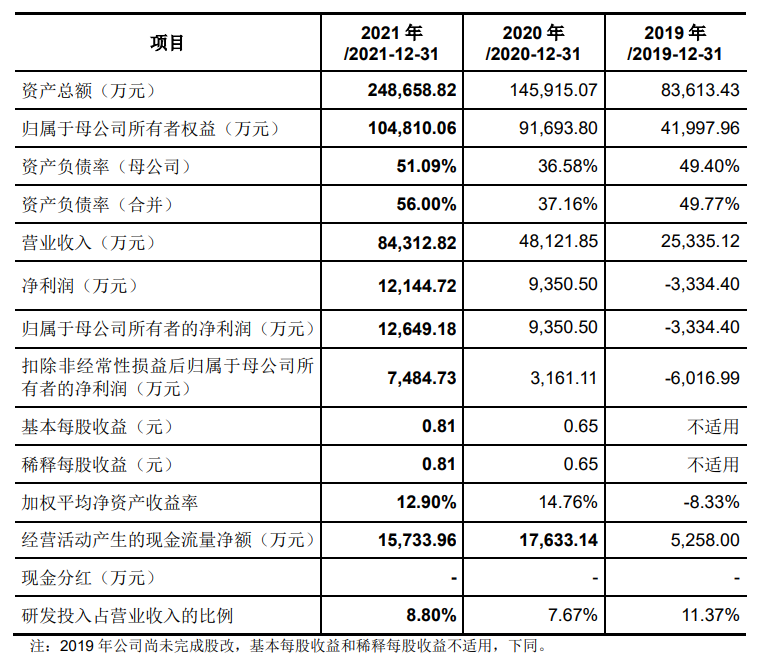
毕得医药科创板IPO申请上会 完成两轮问询回复
-
观典防务正式终止北交所上市 A股“转板第一股”诞生
-
思源电气盘中创60日新低,东吴证券一周前给出“买入”评级,目标价40.48元
-
4月26日分众传媒盘中创60日新低,东方红睿玺三年定开混合A基金重仓该股
-
4月26日思源电气盘中创60日新低,兴全新视野定开混合基金重仓该股